اتم پرتوزا چیست و چه ویژگی هایی دارد؟ – به زبان ساده
اتم رادیو اکتیو که با نامهای هسته پرتوزا (رادیو نوکليد) یا رادیوایزوتوپ هم شناخته میشود، اتمی با تعداد نوترون زیاد و هسته سنگین است که در شرایط عادی دچار واپاشی هسته شده و نوترونهای خود را از دست میدهد تا به اتمی پایدارتر تبدیل شود. طی این فرآیند، هسته اتم پرتوهایی با فرکانس بالا و طول موج کوتاه را تولید میکند و به همین دلیل به آن اتم پرتوزا گفته میشود. در این مطلب از مجله فرادرس میآموزیم اتم پرتوزا چیست و چه ویژگیهایی دارد.
- میآموزید اتم پرتوزا چیست و چه ویژگیهایی دارد.
- با مثالهای مختلف اتم پرتوزا آشنا میشوید.
- دلیل پرتوزایی اتمها و تفاوت آنها با اتم خنثی را درک میکنید.
- یاد میگیرید ایزوتوپ پرتوزا چیست و چگونه پایدار میشود.
- با انواع واکنشهای واپاشی پرتوزا آشنا میشوید.
- خطرات، منابع و کاربردهای اتم پرتوزا را میشناسید.


در ابتدای این مطلب میآموزیم اتم پرتوزا چیست. سپس ویژگیهای اتم پرتوزا و مثالهایی از آن را بررسی میکنیم. در ادامه، دلیل پرتوزایی اتم را آموخته و با مفهوم اتم خنثی آشنا میشویم. پس از آن با مفاهیم ایزوتوپ پرتوزا و پایدار شدن اتم پرتوزا آشنا شده و واکنش واپاشی پرتوزا را میشناسیم. همچنین، با روش تشخیص نوع واپاشی اتم پرتوزا، خطرات اتم پرتوزا و منابع و کاربرد این اتمها نیز آشنا میشویم. با مطالعه این مطلب تا انتها میتوانید به شکلی کامل بیاموزید اتم پرتوزا چیست.
اتم پرتوزا چیست؟
اتم پرتوزا (رادیواکتیو) اتمی است که هستهای ناپایدار دارد و انرژی اضافی خود را به صورت امواج یا پرتوهای الکترومغناطیسی با انرژی زیاد آزاد میکند. این ناپایداری هسته اتم معمولا به دلیل تعداد زیاد نوترون هسته (یا زیاد بودن نسبت پروتونها به نوترونهای هسته) اتفاق میافتد. اتم پرتوزا طی واکنش هستهای به نام واپاشی هستهای، انرژی زیاد حاصل از جرم زیاد نوترونها را از دست میدهد. همچنین طی این فرآیند تعدادی از نوترونهای هسته نیز از آن جدا میشوند.
اتمهای پرتوزا مانند هر اتم دیگری میتوانند به شکل گاز، مایع یا جامد باشند. اتم پرتوزا با نامهای زیر نیز شناخته میشود.
- عنصر پرتوزا
- مواد پروتوزا
- هسته پرتوزا
- هسته ناپایدار
- اتم رادیواکتیو
- هسته رادیواکتیو
- نوکلئید پرتوزا
ویژگی اتم پرتوزا
اتمهای پرتوزا ویژگیها و خواص منحصر به فردی دارند که وجود آنها باعث تمایز آنها از اتمهای خنثی و پایدار میشوند. این ویژگیها مواردی مانند هسته ناپایدار، پرتوزایی، داشتن نیمه عمر و .. است. این موارد در ادامه توضیح داده میشود.
هسته ناپایدار
تمام اتمها به جز سادهترین ایزوتوپ هیدروژن، پروتیوم، شامل پروتون و نوترون در هسته خود هستند. در بیست عنصر اول، تعداد پروتونها و نوترونها تقریبا برابر است، اما در عناصر سنگینتر، نوترونها سریعتر از پروتونها افزایش مییابند. هر پروتون دارای بار مثبت است و این بار در اتمی مانند اتم هیدروژن پایدار است. اما در هستههای دیگر، نیروی دافعه بین پروتونها میتواند هسته را از هم بپاشد. نوترونها با خنثی کردن یا کاهش این نیرو به پایدار ماندن هسته کمک میکنند.
وقتی تعداد پروتونها زیاد شود، نسبت یک به یک نوترونها به پروتونها دیگر کافی نیست و نوترونهای بیشتری برای حفظ ثبات لازم است. به همین دلیل، در عناصر بالاتر از کلسیم تعداد نوترونها بیشتر از پروتونها است. همه عناصر با عدد اتمی بالاتر از پولونیوم (۸۴) ناپایدار و رادیواکتیو هستند. این عناصر طی فرآیند واپاشی پرتوزا پایدار میشوند.
پرتوزایی
اتم پرتوزا به دلیل وجود هسته ناپایدار، دچار واپاشی پرتوزا میشود. در این فرآیند، هسته ناپایدار بهطور خودبهخود به یک هسته پایدارتر تبدیل شده و تابش منتشر میکند. واپاشی رادیواکتیو به سه نوع اصلی تقسیم میشود.
- واپاشی آلفا
- واپاشی بتا
- واپاشی گاما
این موارد در قسمتهای بعد توضیح داده میشوند.
نیمه عمر چیست؟
نیمه عمر مدت زمانی است که طی آن نیمی از مقدار یک ماده در یک فرآیند فروپاشی پیوسته تجزیه یا مصرف میشود. رایجترین روش برای توصیف عناصر رادیواکتیو، نیمه عمر آنها است که گاهی «طول عمر» نیز نامیده میشود. به عنوان مثال، نیمهعمر ایزوتوپ توریم - ۲۲۶ برابر با ۳۰.۹ دقیقه است. نیمهعمر اورانیوم - ۲۳۵ برابر با سال و نیمهعمر اورانیوم - ۲۳۸ حتی طولانیتر و برابر با سال است.
تابش یونیزاسیون
اتم پرتوزا میتواند از خود تابش یونشی منتشر کند. این تابش انرژی کافی برای جدا کردن الکترونها از اتمها و ایجاد یونها دارد. به همین دلیل به این تابش، تابش یونیزاسیون (Ionizing radiation) گفته میشود. این تابش میتواند برای موجودات زنده مضر باشد، زیرا قادر است به سلولها و DNA آسیب برساند.
یادگیری علوم هشتم با فرادرس
برای درک بهتر این موضوع که اتم پرتوزا چیست، ابتدا باید با مفاهیمی چون عدد جرمی، مدلهای اتمی و نظریه اتمی، ایزوتوپها، یونها و واکنشهای شیمیایی آشنا شوید. پیشنهاد میکنیم برای آشنایی بیشتر با این مفاهیم، به مجموعه فیلم آموزش دروس پایه هشتم، بخش شیمی مراجعه کنید که با زبانی ساده ولی کاربردی به توضیح این موارد میپردازد.

همچنین، با مراجعه به فیملمهای آموزش فرادرس که در ادامه آورده شده است، میتوانید به آموزشهای بیشتری در زمینه اتم پرتوزا دسترسی داشته باشید.
- فیلم آموزش علوم تجربی پایه هفتم فرادرس
- فیلم آموزش علوم تجربی پایه هشتم بخش فیزیک فرادرس
- فیلم آموزش علوم تجربی پایه نهم بخش شیمی فرادرس
مثال اتم پرتوزا
در قسمت قبل آموختیم مفهوم اتم پرتوزا چیست. بسیاری از اتمها به صورت طبیعی پرتوزا هستند و برای رسیدن به پایداری، ذرات پرانرژی تابش میکنند. برخی از رایجترین مثالهای اتم پرتوزا مواردی مانند اورانیوم - ۲۳۵، و ... هستند.
تعداد اتمهای رادیواکتیو نسبت به اتمهای خنثی بسیار کم است. برخی از عناصر رادیواکتیو شناخته شده در ادامه معرفی شده است.
- اورانیوم
- پلوتونیوم
- کربن - ۱۴
- پولونیوم
- رادیوم
- رادون
- توریم
- رادون
تقریبا همه عناصر سنگینتر از اورانیوم در سری اکتینیدها مصنوعی هستند و در آزمایشهای فیزیک پرانرژی ساخته شدهاند. همچنین صدها ایزوتوپ شناختهشده از عناصر سبکتر نیز به طور مصنوعی تولید شدهاند. این ایزوتوپها در واکنشهای هستهای ساخته میشوند که در آن هستههای پایدار با ذرات پرانرژی در شتابدهندهها و راکتورهای هستهای بمباران میشوند.
دلیل پرتوزایی اتم چیست؟
دلیل پرتوزایی اتم این است که تعادل بسیار حساس بین نیروهای اجزای تشکیل دهنده اتم است که اتم را پایدار میکند. اگر این تعادل بین نیروهای بین ذرهها به هر دلیل (به صورت طبیعی یا در آزمایشگاه) بر هم بخورد، اتم ناپایدار شده و انرژی ساطع میکند تا دوباره به حالت پایدار برسد. در اتمهای پرتوزا این پدیده اغلب به صورت طبیعی انجام شده و پس از پرتوزایی اتم، اتم جدیدی با تعداد نوترون، الکترون یا پروتون جدید و متفاوت تشکیل میشود.
اگر تا اینجای مطلب را مطالعه کردهاید با ساختار اتم پرتوزا و ویژگیهای آن آشنا شدهاید. در ادامه این مطلب نیز به بررسی واکنشها و کاربردهای این اتمها میپردازیم.
پیشنهاد میکنیم برای مطالعه بیشتر این نوع مطالب و دسترسی همیشگی و رایگان به آنها در موبایل خود، اپلیکیشن رایگان مجله فرادرس را نصب کنید تا همیشه به مطالب مجله فرادرس دسترسی داشته باشید.
برای نصب اپلیکیشن رایگان مجله فرادرس، کلیک کنید.
پرتوهای مختلف حاوی انرژی از اتمهای پرتوزا ساطع میشوند. بسیاری از این پرتوزاییها به صورت طبیعی و در شرایط استاندارد صورت میگیرد. اتمها از تجمع پروتونها و نوترونها در هسته و الکترونهایی که اطراف هسته در حرکت هستند تشکیل شدهاند. بسیاری از اتمها پایدار هستند و نسبت مناسبی از نوترون و پروتون را در هسته خود دارند. اما در برخی از اتمها نسبت نوترون به پروتون بسیار زیاد میشود. در این صورت، انرژی هسته بسیار زیاد شده و پرتوزا میشود.
پس از اینکه اتم پرتوزا دچار واپاشی شده و انرژی را آزاد میکند، ساختار هسته اتم تغییر میکند و یک اتم جدید با ساختار جدید تشکیل میشود. به این فرآیند واکنش هستهای گفته میشود. انرژی آزاد شده با نام پرتوزایی یونش شناخته میشود. زیرا این پرتوها به اندازهای انرژی دارند که بتوانند الکترونهای موجود در ساختار اتم را از آن جدا کرده و اتم را به یون تبدیل کنند.
انرژی هسته ای چیست؟
انرژی هستهای به انرژی بسیار قوی بین ذرات سازنده هسته اتم گفته میشود. این انرژی معمولا بسیار زیاد است و نمیتوان به راحتی بر آن غلبه کرد. انرژی هستهای شامل برهمکنش الکترومغناطیسی بین پروتون - پروتون، پروتون - نوترون و نوترون - نوترون است. انرژی بسیار زیاد هسته اتم و پایداری آن بیشتر به دلیل وجود نوترونهای هسته است که ذرات هسته را در فاصله بسیار کم و متمرکز در کنار هم قرار میدهد و مانع از واپاشی هسته به دلیل دافعه بین پروتونهای مثبت میشود.
اتم خنثی چیست؟
اتم خنثی اتمی است که تعداد برابری پروتون و نوترون دارند. برای به دست آوردن و فهمیدن ساختار اتم میتوان به جدول تناوبی عناصر مراجعه کرد. در جدول تناوبی عناصر میتوان عدد اتمی، که تعداد پروتون اتم و عدد جرمی که مجموع تعداد پروتون و نوترون اتم را مشخص میکند را یافت. همچنین، در اتم خنثی، تعداد اکترونها و پروتونهای اتم برابر است بنابر این ساختار اتم مشخص میشود.
برای مثال اتم نیتروژن در حالت خنثی به شکل زیر است.
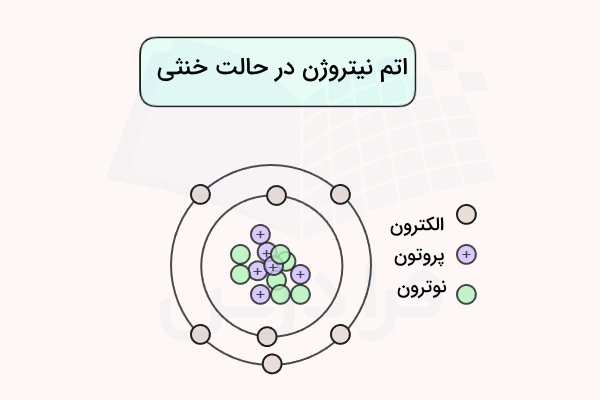
ایزوتوپ پرتوزا چیست؟
ایزوتوپ پرتوزا که با نام رادیونوکلئید نیز شناخته میشود، اتمهای پرتوزایی هستند که تعداد نوترونهای متفاوتی از اتم پایدار خود دارند. برای مثال، کربن - ۱۲، فرم پایدار اتم کربن است. اما اتم کربن - ۱۴ که ۲ نوترون بیشتر دارد، فرم پرتوزای اتم کربن است که از خاصیت پرتوزایی آن در صنعتهای بسیاری استفاده میشود.
ایزوتوپ چیست؟
ایزوتوپها اتمهایی سهتند که تعداد پروتون برابر اما تعداد نوترون نابرابر دارند. این اتمها در واقع ایزوتوپهای یک عنصر با تعداد پروتون مشخص را تشکیل میدهند و فراوانی آنها بر روی زمین متفاوت است. برای مثال، اتم هیدروژن که در حالت خنثی یک الکترون و یک پروتون دراد، ۷ ایزوتوپ با تعداد نوترونهای مختلف نیز دارد. بسیاری از این ایزوتوپها به دلیل نسبت زیاد نروتون به پروتون پرتوزا هستند.
پایدار شدن اتم پرتوزا چیست؟
اتم پرتوزا با تابش انرژی، تلاش میکند به حالت پایدار برسد. این اتمها با پرتوزایی و از دست دادن مقدار نوترون و جرم، به اتم جدیدی تبدیل میشوند. این فرآیند با نام واپاشی پرتوزا (واپاشی رادیواکتیو) شناخته میشود و تا زمانی ادامه پیدا میکند که نیروهای بین ذرات تشکیل دهنده هسته اتم به پایداری و تناسب برسند.
به مجموعه تغییراتی که یک عنصر پرتوزا بهتدریج پشت سر میگذارد، زنجیره واپاشی گفته میشود.
واکنش واپاشی پرتوزا
واکنش واپاشی پرتوزا یکی از مهمترین واگنشهایی اس که برای اتمهای پرتوزا به شکل طبیعی صورت میگیرد. واپاشی پرتوزا نسبت به نوع تابشی که اتم انجام میدهد میتواند انواع مختلفی داشته باشد. این انواع در ادامه نام برده شدهاند.
- واپاشی آلفا
- واپاشی بتا
- واپاشی گاما
- واپاشی پوزیترون
- واپاشی دام اندازی الکترون
- و ...
محصول یک فرایند واپاشی رادیواکتیو که «هسته دختر» ایزوتوپ اولیه نامیده میشود، ممکن است خود ناپایدار باشد. در این صورت، آن نیز واپاشی میکند. این روند ادامه پیدا میکند تا در نهایت یک هسته پایدار تشکیل شود. در ادامه میآموزیم هر یک از این فرایندها برای اتم پرتوزا چیست.
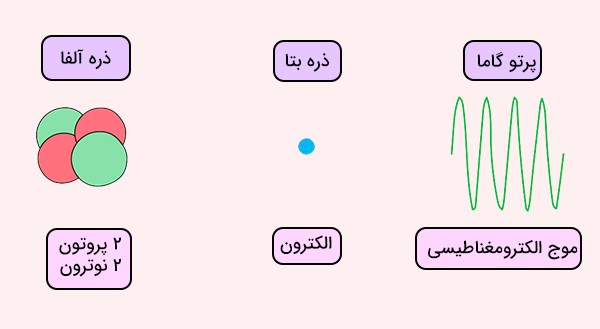
واپاشی آلفا
واکنش واپاشی آلفا واکنشی است که طی آن اتم پرتوزا با ساطع کردن پرتو آلفا به پایداری میرسد. پرتو آلفا (ذره الفا) از دو نوترون و دو پروتون تشکیل شده است. به این ترتیب، ذره آلفا، دارای بار مثبت ۲+ است. ذره آلفا ذرهای بسیار سنگین و پر انرژی است که از بسیاری از مواد عبور نمیکند و نمیتواند در آنها نفوذ کند.
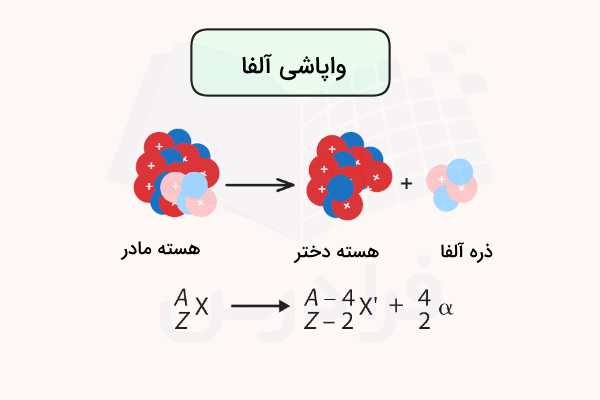
یک قطعه کاغذ یا لایه بیرونی پوست میتواند از نفوذ ذره آلفا جلوگیری کند. ذراتی که پرتو آلفا ساطع میکنند میتوانند در صورت بلع یا ورود به خون بسیار خطرناک باشند. معادله واکنش واپاشی آلفا به شکل زیر است.
در این واکنش، عدد اتمی هسته دختر ۲ واحد و عدد جرمی آن ۴ واحد کاهش مییابد.
چه موادی دچار واپاشی آلفا میشوند؟
مواد پرتوزا که در آنها، نسبت نوترون به پروتون کم و بسیار پایین است دچار واپاشی آلفا میشوند. در ادامه، برخی از موادی که دچار واپاشی آلفا میشوند به همراه واکنش هستهای مربوط به آنها آورده شده است.
- واپاشی آلفا اورانیوم - ۲۳۵
- واپاشی آلفا رادیوم - ۸۸
- واپاشی آلفا رادون - ۸۶
- واپاشی آلفا پولونیوم - ۸۴
- واپاشی آلفا امریسیم - ۹۵
واپاشی بتا
واکنش واپاشی بتا واکنشی است که طی آن اتم پرتوزا با از دست دادن یک ذره بتا به پایداری میرسد. ذره بتا ذرهای است که از تبدیل یک نوترون به یک پروتون و الکترون تشکیل میشود. طی این واکنش، پروتون در هسته اتم باقی مانده و الکترون از آن جدا میشود. در نتیجه، ذره بتا دارای بار الکتریکی ۱- است. این فرآیند تعداد نوترونها را کاهش داده و تعداد پروتونها را افزایش میدهد.
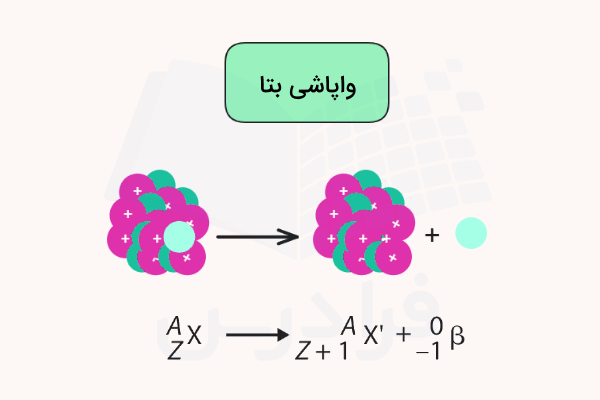
سرعت هر ذره بتا به مقدار انرژی آنها بستگی دارد و برای هر ذره بتا متفاوت است. یک یا دو لایه پارچه یا موادی مانند آلومینیوم میتوانند مانع نفوذ و عبور ذرات بتا شوند. این ذرات میتوانند باعث آسیب به پوست (سوختگی) شوند. معادله واکنش واپاشی بتا به شکل زیر است.
چه ذراتی دچار واپاشی بتا میشوند؟
اتم پرتوزایی که در آن تعداد نوترونها به الکترونها بسیار زیاد است، دچار واپاشی بتا میشوند تا به پایداری برسند. در واقع واپاشی بتا با تبدیل یک نوترون به یک پروتون و خارج کردن یک الکترون، همزمان تعداد نوترونها را کاهش داده و تعداد پروتونها را افزایش میدهد. بدین ترتیب، نسبت نوترون به پروتون کاهش یافته و اتم پایدارتر میشود.
واپاشی گاما
واکنش واپاشی گاما واکنشی است که طی آن، ذرات گاما از هسته اتم جدا میشوند. ذرات گاما جرم و نوترون و پروتون و بار الکتریکی ندارند و انرژی خالص الکترومغناطیسی هستند. این ذرات با سرعت بسیار بالایی (نزدیک به سرعت نور) حرکت کرده تنها با موادی مانند سرب یا چندین متر بتن میتوان جلوی نفوذ آنها را گرفت.
این ذرات به شدت پرانرژی میتوانند به پوست، لباس و ارگانهای موجودات آسیب بزنند. معادله واکنش واپاشی گاما به شکل زیر است.
$$^{A}_{Z}\textrm{X*}\rightarrow\,^{A}_{Z}\textrm{X}+^{0}_{0}\gamma$$
چه موادی دچار واپاشی گاما میشوند؟
اتم پرتوزایی که در آنها انرژی به حدی زیاد است که با تابش آلفا و بتا به پایداری نمیرسند، دچار واپاشی گاما میشوند.
گرفتن (دام اندازی) الکترون
راه دیگری که یک نوکلید میتواند نسبت نوترون به پروتون خود را افزایش دهد، گرفتن الکترون است. در این فرآیند، یک الکترون از مدار داخلی اتم توسط هسته جذب میشود و با یک پروتون ترکیب شده تا یک نوترون بسازد. برای مثال، نقره - ۱۰۶ از طریق گرفتن الکترون به پالادیوم - ۱۰۶ تبدیل میشود.
در این واپاشی، عدد اتمی یک واحد کاهش مییابد، اما عدد جرمی بدون تغییر باقی میماند. معادله واکنش واپاشی گرفتن الکترون به شکل زیر است.
واپاشی پوزیترون
واکنش واپاشی پوزیترون واکنش است که طی آن یک ذره پوزیترون آزاد میشود. ذره پوزیترون ذرهای است که جرم آن با جرم الکترون برابر اما بار آن مخالف بار الکترون است. بنابراین این نشر دقیقا مخالف واپاشی بتا است.
واکنش واپاشی پوزیترون به شکل زیر است.
$$^{1}_{1}\textrm{p}^+\rightarrow^{1}_{0}\textrm{n}+\,^{0}_{+1}\beta^+$$
چه اتم هایی دچار واپاشی پوزیترون میشوند؟
اتمهایی که در آنها نسبت نوترون به پروتون کم است، با تبدیل یک پروتون به نوترون و پوزیترون به پایداری میرسند. اتمهای پرتوزا میتوانند طی برخی دیگر از واکنشهای هستهای نیز تابشهای پرانرژی را از خود ساطع کنند. پیشنهاد میکنیم برای آشنایی بیتشر با این واکنشها، مطلب واکنش هستهای مجله فرادرس را مطالعه کنید.

پیشنهاد میکنیم برای درک بهتر انواع پرتوها و ویژگیهای آنها، فیلم آموزش فیزیک پرتوها فرادرس که لینک آن در ادامه آورده شده است را مشاهده کنید.
واپاشی اتم اورانیوم
اورانیوم اتمی پایدار است که بالاترین عدد اتمی را دارد. این عنصر به صورت طبیعی به صورت ایزوتوپ اورانیوم - ۲۳۸ وجود دارد. تنها درصد بسیار کمی از اورانیومی که به صورت طبیعی وجود دارد، با جرم اتمی متفاوتی یافت میشود که مربوط به ایزوتوپ اورانیوم - ۲۳۵ است.
اورانیوم - ۲۳۸ به صورت طبیعی دچار واپاشی آلفا شده و به توریوم - ۲۳۴ تبدیل میشود. واکنش این واپاشی به شکل زیر است.
اورانیوم - ۲۳۵ نیز دچار واپاشی میشود. اتم اورانیوم میتواند طی واپاشیهای پی در پی آلفا و بتا به اتمهای دیگری تبدیل شده و انرژی بسیاری را تولید کنید. تصویر زیر، نمایش سری واپاشی اتم اورانیوم است.

خطرات اتم پرتوزا
در قسمتهای قبل آموختیم اتم پرتوزا چیست. اتم پرتوزا میتواند بسته به تابشی که طی فرآیند واپاشی انجام میدهد خطراتی را برای انسان و جانوران به همراه داشته باشد. همانطور که در قسمتهای قبل اشاره شد، کمخطرترین ذره تابش شده طی پرتوزایی، ذره آلفا و خطرناکترین آنها، پرتو گاما است.

در ادامه برخی از خطرات اتم پرتوزا را توضیح میدهیم.
- مسمومیت ناشی از تابش: در صورت قرار گرفتن در معرض تابش زیاد، فرد ممکن است دچار تهوع، استفراغ، اسهال، خستگی و ریزش مو شود.
- سرطان: تابش میتواند احتمال ابتلا به انواع سرطانها را افزایش دهد.
- نقصهای مادرزادی: زنان باردار در معرض تابش شدید ممکن است فرزندی با نواقص مادرزادی به دنیا بیاورند.
- آلودگی محیط زیست: واپاشی رادیواکتیو میتواند محیطزیست را آلوده کرده و آن را برای انسانها و دیگر موجودات زنده ناایمن کند.
محافظت در برابر اتم پرتوزا
برای کاهش خطرات اتم پرتوزا و حفاظت در برابر تشعشعات آنها میتوان اقدامات ایمنی زیر را انجام داد.
- پوشش حفاظتی: باید از محافظهای مناسب برای جلوگیری از انتشار تابش استفاده شود.
- تهویه مناسب: فضاهایی که عناصر رادیواکتیو در آنها استفاده میشوند، باید دارای جریان هوای کافی باشند تا از تجمع گازهای رادیواکتیو جلوگیری شود.
- پایش مستمر تابش: بررسی مداوم عناصر رادیواکتیو لازم است تا اطمینان حاصل شود تابشی نشت نمیکند.
- آموزش کارکنان: افرادی که با این مواد کار میکنند باید با روشهای ایمن کار کردن با اتم پرتوزا آشنا باشند.
منابع اتم پرتوزا چیست؟
تقریبا تمامی عناصر ایزوتوپهای رادیواکتیو شناختهشده دارند. با این حال، تنها تعداد کمی از ایزوتوپهای طبیعی بهصورت رادیواکتیو هستند. اکثریت عناصر رادیواکتیو، عناصر ساختهشده توسط انسان هستند که از طریق واکنشهای سنتز هستهای در آزمایشهای برخورد ذرات پرانرژی تولید و شناسایی شدهاند.
در ادامه منابع برخی از اتمهای پرتوزا معرفی شده است.
- کربن - ۱۴: تولید طبیعی در جو زمین بر اثر برخورد پرتوهای کیهانی با هستههای کربن-۱۲ در دی اکسید کربن هوا
- اورانیوم: وجود طبیعی در پوسته زمین و استخراج از سنگ معدن پیچبلند
- توریم: وجود طبیعی و استخراج تجاری از معدن مونازیت
- رادیوم: حاصل فروپاشی رادیواکتیو اورانیوم در سنگهای معدنی مانند پیچبلند
- رادون: تولید طبیعی بر اثر فروپاشی رادیواکتیو رادیوم
- پولونیوم: وجود طبیعی به عنوان محصول فروپاشی عناصر سنگینتر مانند اورانیوم
- استاتین: وجود طبیعی بسیار نادر، حاصل زنجیرههای فروپاشی هستهای
- پروتاکتینیوم: وجود طبیعی به مقدار کم در زنجیره فروپاشی اورانیوم
همانطور که قبلا اشاره شد، سایر اتمهای پرتوزای عناصر سنگین به صورت مصنوعی و در آزمایشگاه تولید میشوند.
کاربرد اتم پرتوزا چیست؟
در این مطلب از مجله فرادرس آموختیم اتم پرتوزا چیست. برخی از اتمهای پرتوزا ابزارهای ارزشمندی در پزشکی تشخیصی و دیگر کاربردهای علمی هستند، اما بیشتر آنها تنها بهعنوان دادههای تجربی برای مطالعات دانشگاهی و مدلهای نظری رفتار اتمها اهمیت دارند. در ادامه برخی از کاربردهای این عناصر را توضیح میدهیم.

پزشکی
تصویربرداران پزشکی از اطلاعات مربوط به نیمهعمر استفاده میکنند تا زمان تابش فیلمهای اشعه ایکس و اسکنهایی که با دیگر انواع تابش یونساز انجام میشود را تنظیم کنند. همچنین برخی از این عناصر در پرتو درمانی برای درمان سرطان مورد استفاده قرار میگیرند. داروهای رادیوایزوتوپی نیز از دیگر کاربردهای اتم پرتوزا در پزشکی هستند. این داروها شامل ایزوتوپهای رادیواکتیو هستند و هم در تشخیص و هم در درمان بیماریها استفاده میشوند.
باستان شناسی
نیمهعمر عناصری که به کندی فروپاشی میشوند، مانند اورانیوم-۲۳۸ و کربن-۱۴، برای تعیین سن مواد آلی به کار میرود.
انرژی هسته ای
از برخی از اتمهای پرتوزا به عنوان سوخت در راکتورهای هستهای برای تولید برق استفاده میشوند. انرژی هستهای منبعی قابل اعتماد و کارآمد است که میزان کمی از گازهای گلخانهای را تولید میکند.
رادیوگرافی صنعتی
در صنعت، از عناصر رادیواکتیو برای بررسی و کشف نقصها در مواد و قطعات استفاده میشود. این روش کمک میکند تا ترکها یا حفرههای داخلی بدون نیاز به باز کردن کامل قطعه شناسایی شوند. همچنین از ایزوتوپهای رادیواکتیو برای اندازهگیری ضخامت، چگالی و سطح مواد در فرآیندهای صنعتی استفاده میشود. به علاوه، ایزوتوپهای رادیواکتیو بهعنوان ردیاب برای مطالعه جریان مایعات، گازها و جامدات در فرآیندهای صنعتی بهکار میروند.
آشکارساز دود
برخی آشکارسازهای دود از عناصر رادیواکتیو برای تشخیص حضور دود در هوا استفاده میکنند. تابش این عناصر با ورود دود تغییر میکند و باعث فعال شدن صدای هشدار میشود.
تحقیقات علمی
از اتم پرتوزا در علوم فیزیک، شیمی و زیست شناسی برای مطالعه ساختار اتم، ردیابی واکنشهای شیمیایی و مطالعه فرآیندهای زیستی استفاده میشود.
اکتشافات فضایی
در فضاپیماها، عناصر رادیواکتیو بهعنوان منبع انرژی پایدار و طولانیمدت برای ماموریتهایی که دور از خورشید انجام میشوند، استفاده میشوند.