هیدروکربن حلقوی چیست؟ – ساختار و خواص به زبان ساده
هیدروکربنها ترکیباتی هستند که از اتمهای کربن و هیدروژن تشکیل شدهاند. این ترکیبات به دلیل ظرفیت چهارتایی کربن میتوانند انواع مختلف ساختار را داشته باشند. هیدروکربنهای حلقوی، هیدروکربنهایی هستند که در آنها اتمهای کربن در یک ساختار حلقوی به هم متصل شدهاند. این ترکیبات میتوانند پیوندهای یگانه، دوگانه یا سهگانه داشته باشند. در این مطلب از مجله فرادرس میآموزیم هیدروکربن حلقوی چیست و چه خواص و ساختاری دارد.
- میآموزید هیدروکربن حلقوی چیست و چه ساختاری دارد.
- با انواع هیدروکربن حلقوی و ویژگیهای آنها آشنا میشوید.
- انواع ترکیبات حلقوی آلی و غیرآلی را میشناسید.
- با تنش و کرنش در ترکیبات حلقوی و تفاوت آنها آشنا میشوید.
- میتوانید استریوشیمی و نمایش هیدروکربن حلقوی را تشخیص دهید.
- انواع واکنشهای هیدروکربن حلقوی را یاد میگیرید.
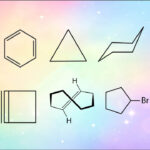
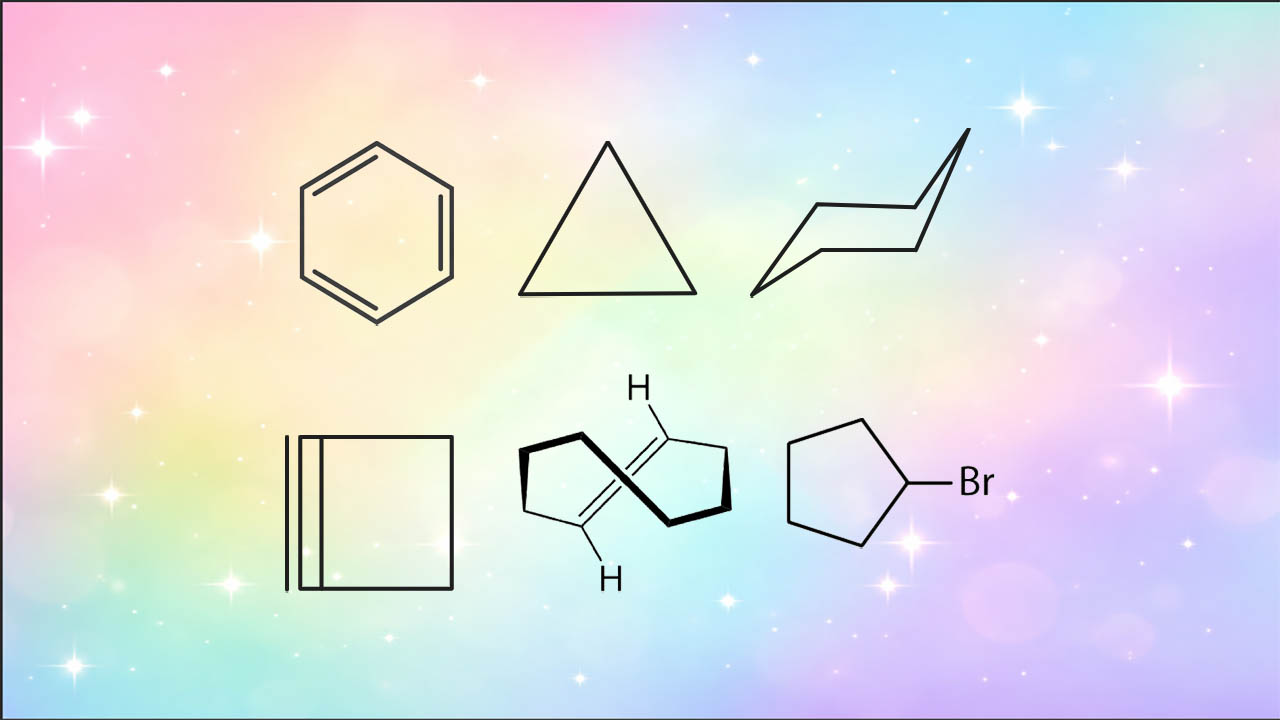
در ابتدای این مطلب میآموزیم هیدروکربن حلقوی چیست. سپس انواع هیدروکربن حلقوی را آموخته و ترکیبات حلقوی را در شیمی بررسی میکنیم. سپس خواص و ساختار سیکلوآلکانها، سیکلوآلکنها، سیکلوآلکینها و ترکیبات آروماتیک را میآموزیم. در ادامه، با تنش و کرنش هیدروکربنهای حلقوی آشنا شده و نمایش و واکنش آنها را میآموزیم. با مطالعه این مطلب تا انتها میتوانید به شکلی کامل بیاموزید هیدروکربن حلقوی چیست.
هیدروکربن حلقوی چیست؟
هیدروکربن حلقوی ترکیبی شیمیایی متشکل از کربن و هیدروژن است که در آن اتمهای کربن در ساختاری حلقوی به هم متصل شدهاند. این ترکیبات میتوانند از ۳ تا تعداد بالایی کربن داشته باشند. مرتبه پیوند در این ترکیبات میتواند از نوع یگانه، دوگانه یا سهگانه باشد. این ترکیبات میتوانند به سایر گروههای مولکولی وصل شده و هیدروکربنهای حلقوی شاخهدار بسازند یا خود بهعنوان شاخه فرعی به سایر هیدروکربنها متصل شوند.
ترکیبات هیدروکربن حلقوی که دارای تعداد مشخصی پیوند دوگانه در ساختار خود هستند و از قانون هوکل پیروی میکنند، ترکیبات هیدروکربن آروماتیک را تشکیل میدهند. این ترکیبات که ساختاری رزونانسی دارند، در بسیاری از مواد آلی مانند ترکیبات نفتی دیده میشوند و یکی از مهمترین دستههای هیدروکربنهای حلقوی هستند. در تصویر زیر، ساختار برخی از هیدروکربنهای حلقوی نمایش داده شده است.
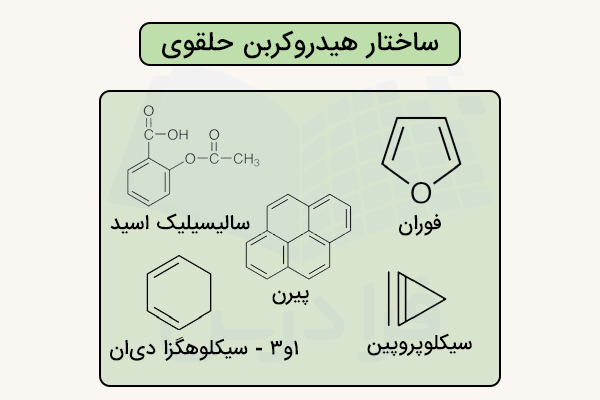
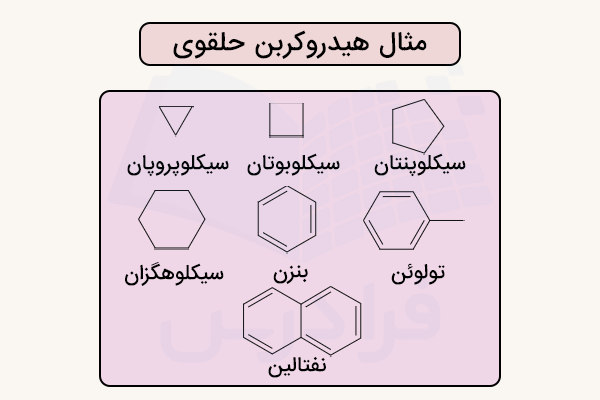
مثال هیدروکربن حلقوی چیست؟
بسیاری از موادی که هر روز با آنها سروکار داریم، مانند بسیاری از پلاستیکها، مواد نفتی و ... شامل حلقههای هیدروکربنی هستند. از مهمترین ترکیبات حلقوی هیدروکربنی میتوان به موارد زیر اشاره کرد. در ادامه، نام و ساختار برخی از هیدروکربنهای حلقوی ارائه شده است.
- سیکلوپروپان (Cyclopropane)
- سیکلوبوتان (Cyclobutane)
- سیکلوپنتان (Cyclopentane)
- سیکلوهگزان (Cyclohexane)
- بنزن (Benzene)
- تولوئن (Toluene)
- نفتالین (Naphthalene)
یادگیری شیمی یازدهم با فرادرس
برای درک بهتر اینکه هیدروکربن حلقوی چیست، ابتدا باید با مفاهیم هیدروکربن، مواد آلی، ساختار لوویس، ایزومرها و پیوند شیمیایی آشنا شویم. پیشنهاد میکنیم برای یادگیری بهتر این مفاهیم، به مجموعه فیلمهای آموزش پایه یازدهم فرادرس، بخش شیمی مراجعه کنید که با زبانی ساده ولی کاربردی به توضیح این مفاهیم میپردازد.
همچنین، با مشاهده فیلمهای آموزش فرادرس که در ادامه آورده شده است، به آموزشهای بیشتری در مورد هیدروکربن حلقوی دسترسی خواهید داشت.
- فیلم آموزش شیمی ۳ پایه دوازدهم فرادرس
- فیلم آموزش شیمی ۱ پایه دهم فرادرس
- فیلم آموزش شیمی ۱ پایه دهم حل سوالات تشریحی امتحانات نهایی فرادرس
انواع هیدروکربن حلقوی
در قسمت قبل آموختیم هیدروکربن حلقوی چیست. هیدروکربنهای حلقوی بر اساس مرتبه پیوند میتوانند به سیکلوآلکان، سیکلوآلکن یا سیکلوآلکین تقسیم شوند. همچنین این ترکیبات از نظر آروماتیک بودن به دستههای آروماتیک و غیر آروماتیک تقسیم میشوند. در ادامه این دستهبندیها را توضیح میدهیم.
سیکلوآلکان ها
سیکلوآلکانها ترکیبات هیدروکربن حلقوی هستند که بین اتمهای کربن حلقه آنها تمامی پیوندها از نوع یگانه است. سادهترین نوع سیکلوآلکان، سیکلوپروپان است. برخی از مثالهای سیکلوآلکانها در ادامه آورده شده است. سیکلوآلکانهایی که تعداد اتمهای کربن آنها بیش از ۲۰ باشد، معمولا با نام سیکلوپارافین شناخته میشوند. این ترکیبات از نظر فرمول مولکولی، ایزومر آلکنها محسوب میشوند.
این ترکیبات فقط از اتمهای کربن و هیدروژن تشکیل شدهاند و ساختار آنها شامل یک حلقه کربنی است که ممکن است دارای زنجیرههای جانبی نیز باشد. در ترکیبات سیکلوآلکان امکان وجود ایزومرهای سیس و ترانس وجود دارد و واکنشپذیری آنها مشابه آلکانها است. با این وجود، سیکلوآلکانهای کوچکتر (با تعداد اتم کربن کمتر در حلقه) واکنشپذیری بیشتری نسبت به سایر آنها دارند. همانند سایر آلکانها، سیکلوآلکانها ترکیبات هیدروکربن اشباع هستند. فرمول کلی سیکلوآلکانها به صورت زیر است:
در این رابطه، n نشان دهنده تعداد اتمهای کربن و r بیانگر تعداد حلقهها است. اگر تنها یک حلقه در ساختار وجود داشته باشد، فرمول به شکل سادهتر زیر در میآید:
اتمهای کربن در سیکلوآلکانها همچنان دارای هیبریداسیون هستند و زاویه پیوندی ایدهآل آنها برابر ۱۰۹٫۵ درجه است.
نامگذاری سیکلوآلکان ها
سیکلوآلکانهای بدون جانشین که فقط یک حلقه دارند، معمولا با افزودن پیشوند «سیکلو» به نام آلکان خطی هم تعداد کربن نامگذاری میشوند. برای مثال، «سیکلوپروپان» (cyclopropane) با فرمول از «پروپان» (propane) با فرمول گرفته شده است.
اگر تا این قسمت از مطلب را مطالعه کردهاید، با تعریف هیددروکربن حلقوی و ویژگیهای آن آشنا شدهاید. در ادامه مطلب نیز به بررسی بیشتر این مواد میپردازیم.
پیشنهاد میکنیم برای مطالعه بیشتر این نوع مطالب و دسترسی همیشگی و رایگان به آنها در موبایل خود، اپلیکیشن رایگان مجله فرادرس را نصب کنید تا همیشه به مطالب مجله فرادرس دسترسی داشته باشید.
برای نصب اپلیکیشن رایگان مجله فرادرس، کلیک کنید.
در نامگذاری ترکیبات چندحلقهای مانند بیسیکلیکها و اسپایروها، ساختار نام پیچیدهتر است. در این حالت، نام شامل تعداد کل کربنهای ترکیب حلقوی، پیشوندهایی مانند «بیسیکلو» (bicyclo) (در ترکیبات دارای پل) یا «اسپیرو» (spiro) (در ترکیبات چند حلقهای با یک اتم مشترک) برای نشان دادن تعداد حلقهها، و یک بخش عددی است که تعداد کربنهای هر بخش از حلقه (به جز اتمهای اتصال) را مشخص میکند. برای نمونه، ترکیب «بیسیکلو۲و ۲و ۱- هپتان» (bicyclo[2.2.1]heptane) دارای ساختار دوحلقهای مشخص زیر است.
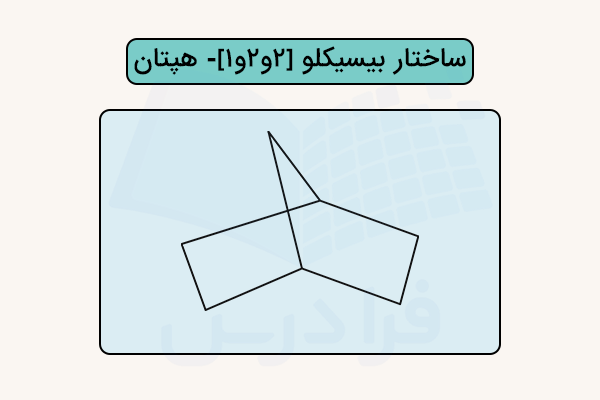
در نامگذاری آیوپاک (IUPAC)، اگر جانشینها یا شاخههایی مانند کلر یا گروه متیل وجود داشته باشد، این اطلاعات نیز به نام افزوده میشود. در مقابل، نامهای رایج کوتاهتر هستند و اطلاعات ساختاری کمتری ارائه میدهند. به طور کلی، سیکلوآلکانها در صنعت نفت با نام «نفتنها» (naphthenes) نیز شناخته میشوند.
خواص سیکلوآلکان ها
سیکلوآلکانها ترکیبات اشباع حلقهای هستند که فقط از پیوندهای C-C و C-H تشکیل شدهاند و از نظر خواص کلی به آلکانها شبیه هستند. اما این ترکیبات به دلیل ساختار حلقهای، نیروهای بین مولکولی قویتری دارند و در نتیجه نقطه جوش و ذوب بالاتری نشان میدهند.
در حلقههای کوچک مثل سیکلوپروپان، کرنش زاویهای باعث افزایش واکنش پذیری و تمایل به باز شدن حلقه میشود. در ادامه مهمترین خواص سیکلوآلکانها را نام بردهایم.
- فقط دارای پیوندهای C-C و C-H هستند و شبیه آلکانها هستند.
- با افزایش سطح تماس مولکولی، نیروهای لاندن قویتری دارند.
- نقطه جوش، نقطه ذوب و چگالی آنها از آلکانهای متناظر بالاتر است.
- حلقههای سیکلوآلکان دارای کرنش واکنشپذیرتر و مستعد باز شدن حلقه هستند.
- نقطه ذوب در آنها به تعداد کربن (زوج یا فرد بودن) وابسته است.
- رفتار فازی آنها به شکل پذیری ساختار در حالت جامد وابسته است.
تولید و کاربرد سیکلوآلکان ها
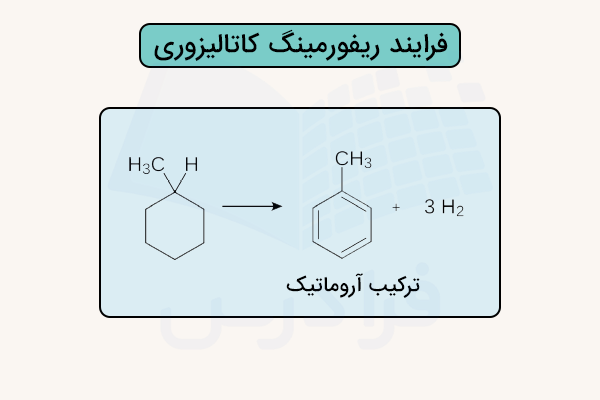
سیکلوآلکانها که به آنها نفتن نیز گفته میشود، در صنعت نفت اهمیت زیادی دارند. در فرایند «ریفورمینگ کاتالیزوری»، این ترکیبات در حضور کاتالیزور و دمای حدود دچار دهیدروژناسیون شده و به ترکیبات آروماتیک تبدیل میشوند. این فرایند برای تولید بنزین با عدد اکتان بالا استفاده میشود.
در یک فرایند صنعتی دیگر، سیکلوهگزانول از اکسایش سیکلوهگزان در حضور هوا و کاتالیزورهایی مانند کبالت به دست میآید. این واکنش همراه با تولید سیکلوهگزانون است و مخلوط حاصل (KA oil) ماده اولیه مهمی برای تولید اسید آدیپیک و در نهایت نایلون است.
سیکلوآلکانهای کوچک، به ویژه سیکلوپروپان، به دلیل کرنش حلقهای پایداری کمتری دارند و واکنش پذیرترند. این ترکیبات برخلاف آلکنها معمولا در واکنش افزایشی الکترون دوست شرکت نمیکنند، بلکه در واکنشهای جانشینی نوکلئوفیلی شرکت کرده و دچار باز شدن حلقه میشوند. بسیاری از سیکلوآلکانها از نفت به دست میآیند یا از طریق هیدروژناسیون ترکیبات غیراشباع و حتی ترکیبات آروماتیک تولید میشوند. همچنین روشهای آزمایشگاهی مختلفی برای ساخت آنها وجود دارد. در ادامه سایر این روشها معرفی شده است.
- واکنشهای حلقهزایی از ترکیبات دو عاملی
- واکنش «آسیلوئین» (Acyloin Condensation)
- واکنش «دیلز-آلدر» (Diels-Alder Reaction) برای تشکیل حلقههای شش کربنه
- واکنشهای سیکلواضافه شدن (۲+۲) (معمولا با نور) برای تشکیل حلقههای چهار کربنه
سیکلوآلکن ها
در قسمت قبل آموختیم خواص سیکلوآلکانها به عنوان هیدروکربن حلقوی چیست. دسته دیگری از ترکیبات حلقوی سیکلو آلکنها هستند. سیکلوآلکنها ترکیبات هیدروکربن حلقوی هستند که در ساختار حلقه آنها حداقل یک پیوند دوگانه وجود دارد. برای مثال، سیکلوهگزن یا سیکلوپروپن از این نوع ترکیبات هستند. این ترکیبات غیرآروماتیک بوده و میتوانند بیش از یک پیوند دوگانه در ساختار خود داشته باشند. واکنشپذیری سیکلوآلکنها از سیکلوآلکانها بیشتر است.
از جمله سیکلوآلکنهای تکحلقهای میتوان به سیکلوپروپن، سیکلوبوتن، سیکلوپنتن، سیکلوهگزن، سیکلوهپتن و سیکلواوکتن اشاره کرد. علاوه بر آنها، آلکنهای دوحلقهای مانند نوربورنان و نوربورنادیان نیز وجود دارند. برخی ترکیبات مهم دیگر مانند متیلنسیکلوهگزن و ۱-متیلسیکلوهگزن، مشتقاتی از سیکلوهگزن هستند که تفاوت آنها در محل قرارگیری پیوند دوگانه است.

مکان قرارگیری پیوندهای دوگانه در ترکیبات آلی حلقوی اهمیت زیادی دارد و میتوان آن را با استفاده از «قانون بردت» (Bredt's rule) پیشبینی کرد. این قانون بیان میکند که تشکیل پیوند دوگانه در برخی موقعیتهای پلدار، به دلیل تنش فضایی شدید، از نظر پایداری امکانپذیر نیست.
نامگذاری سیکلوالکن ها
نامگذاری سیکلوآلکانها مانند سیکلوآلکنها است با این تفاوت که کربنی که روی آن پیوند دوگانه وجود دارد مشخص شده و همچنین نام ترکیب پسوند «-ِن» میگیرد. برای نامگذاری این ترکیبات مانند آلکنهای راست زنجیر عمل کرده و شماره ۱ را به یکی از پیوندهای دوگانه حلقه میدهیم و به سمت نزدیکترین شاخه فرعی یا پیوند دوگانه دیگر شمارهها را ادامه میدهیم. سپس با ذکر نام و شماره و نام شاخههای فرعی، شماره پیوند دوگانه را مینویسیم. سپس قبل از ذکر نام زنجیره اصلی، عبارت «سیکلو» را درج میکنیم.
پیشنهاد میکنیم برای درک بهتر نحوه نامگذاری این ترکیبات، مطلب نام گذاری هیدروکربنها مجله فرادرس که لینک آن در ادامه آورده شده است را مطالعه کنید.
خواص سیکلوآلکن ها
سیکلوآلکنهای حلقه کوچک نسبت به سیکلوآلکانهای هم اندازه، کرنش زاویهای بیشتری (حدود ۲۰ درجه بیشتر) دارند. دلیل این است که زاویه پیوند در آلکنها ۱۲۲ درجه و در آلکانها ۱۱۲ درجه است، بنابراین در حلقههای کوچک، پیوند دوگانه مجبور به فشرده شدن بیشتری شده و کرنش افزایش مییابد.
همچنین، سیکلوآلکنها نسبت به سیکلوآلکانهای هم اندازه، نقطه ذوب پایینتری دارند، چون وجود پیوند دوگانه مانع از فشرده شدن منظم مولکولها میشود. این موادر از نظر خواص فیزیکی شبیه به سیکلوآلکانها هستند و به دلیل وجود پیوند دوگانه، از واکنشپذیری بیشتری برخوردارند. ایزومرهای سیس در سیکلوآلکنها پایدارتر از ترانس هستند، اما این موضوع بیشتر برای ترکیباتی با حداکثر ۱۰ اتم کربن صدق میکند. با افزایش تعداد کربنها، امکان تشکیل ایزومر ترانس نیز بیشتر میشود.
واکنش تولید سیکلوالکن ها
چند روش مهم برای تهیه سیکلوآلکنها وجود دارد که در ادامه معرفی شده است.
- متاتز حلقهزا (Ring-closing metathesis): در این روش، آلکنهای انتهایی با جابهجایی گروهها به یکدیگر متصل شده و یک سیکلوآلکن با پیکربندی E یا Z تشکیل میدهند.
- کاهش برچ (Birch reduction): برای کاهش ترکیبات آروماتیک و تبدیل آنها به سیکلوآلکنها (معمولا سیکلوهگزادیان) به کار میرود.
- واکنش دیلز-آلدر (Diels–Alder reaction): یک دیان مزدوج با یک آلکن واکنش داده و در یک فرایند همزمان، یک سیکلوآلکن تشکیل میدهد.
- واکنشهای حلقهزایی (Cyclization): واکنشهای درونمولکولی که میتوانند سیکلوآلکنهایی مانند سیکلوپنتنون بسازند.
- واکنشهای الکتروسیکلیک (Electrocyclic reactions): با گرما یا نور، یک پیوند پای به پیوند سیگما تبدیل شده و حلقه بسته میشود.
- واکنش مکموری درونمولکولی (Intramolecular McMurry): دو گروه کربونیل در یک مولکول به هم متصل شده و در شرایط مناسب یک سیکلوآلکن تشکیل میدهند.
سیکلوآلکین ها
سیکلوآلکینها ترکیبات هیدروکربنی حلقوی هستند که در ساختار حلقه آنها پیوند سهگانه وجود داشته باشد. این ترکیبات نسبت به دستههای دیگر کمتر رایج هستند. وجود پیوند سهگانه در حلقههای کوچک هیدروکربنی بسیار ناپایدار است به همین علت ساختارهای کوچک سیکلوآلکین اغلب وجود ندارند یا فقط تحت شرایط خاص پایدار میشوند.
فرمول کلی این ترکیبات به صورت است. به دلیل خطی بودن ساختار پیوند ، تشکیل حلقه در این ترکیبات با کرنش زیادی همراه است. بنابراین، سیکلوآلکینها فقط زمانی پایدار هستند که تعداد کربنها به اندازه کافی زیاد باشد تا انعطاف لازم برای این ساختار فراهم شود. کوچکترین سیکلوآلکین پایدار «سیکلوکتین» (cyclooctyne) با فرمول است که میتوان آن را جدا و نگهداری کرد.
با این حال، سیکلوآلکینهای کوچکتر را میتوان به طور موقت در واکنشها تولید و با استفاده از ترکیب شدن با مولکولهای دیگر یا اتصال به فلزات واسطه، پایدار کرد. در تصویز زیر ساختار برخی از سیکلو آلکینها مشخص شده است.
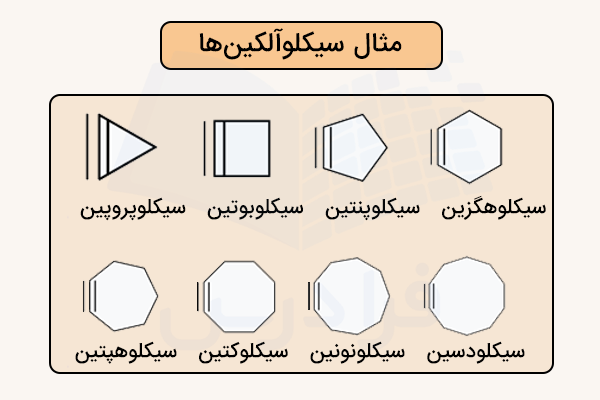
نامگذاری سیکلوآلکین ها
نامگذاری ترکیبات هیدروکربن حلقوی شامل پیوندهای دوگانه یا سهگانه مانند نامگذاری سیکلوآلکانها است. با این تفاوت که سیکلوآلکینها پیشوند و پسوند «سیکلو... -ین» میگیرند. برای درک بهتر این نحوه نامگذاری به ترکیبات زیر دقت کنید.
واکنش پذیری سیکلوآلکین ها
از نظر واکنشپذیری، سیکلوآلکینها مانند آلکینهای خطی در واکنشهای افزایشی شرکت میکنند، اما به دلیل تنش بالا، این واکنشها با شرایط بسیار ملایمتری انجام میشوند. آنها در واکنشهایی مثل دیلز-آلدر، سیکلواضافه شدن ۱٬۳-دو قطبی و هالوژناسیون بسیار فعال هستند.
ترکیبات آروماتیک
تا اینجا آموختیم سه نوع مهم هیدروکربن حلقوی چیست. ترکیبات آروماتیک نیز در دستهبندی هیدروکربن حلقوی قرار میگیرند. ترکیبات آروماتیک، ترکیباتی حلقوی هستند که در ساختار آنها تعداد مشخصی پیوند دوگانه وجود دارد. این ترکیبات میتوانند تکحلقهای یا چندحلقهای باشند. در ترکیبات آروماتیک چندحلقهای، حلقهها پیوند مشترک دارند و این ترکیبات دارای ساختار رزونانسی هستند.
در این ساختار، پیوندهای یگانه و دوگانه بهصورت متناوب در حلقه قرار دارند. معروفترین ترکیب این گروه، بنزن است که از یک حلقه ششضلعی شامل شش اتم کربن تشکیل شده است. برای اینکه یک ترکیب آروماتیک باشد، باید سه شرط کلی را داشته باشد:
- مولکول باید حلقوی باشد.
- هر اتم در حلقه باید دارای اوربیتال p عمود بر صفحه حلقه باشد، بنابراین مولکول باید تخت باشد. این به این معناست که در حلقه نباید اتم کربن خنثی وجود داشته باشد.
- ترکیب باید از قانون هوکل پیروی کند، یعنی تعداد الکترونهای پای آن برابر با باشد.
هیدروکربنهای آروماتیک دارای ویژگیهای شیمیایی خاصی هستند و در کاربردهای مختلف صنعتی و همچنین در زندگی روزمره مورد استفاده قرار میگیرند. همچنین این ترکیبات میتوانند از بههم پیوستن چند حلقه آروماتیک نیز به وجود آمده و ترکیبات چندحلقهای آروماتیک را تشکیل دهند. در تصویر زیر ساختار برخی از ترکیبات آروماتیک نمایش داده شده است.
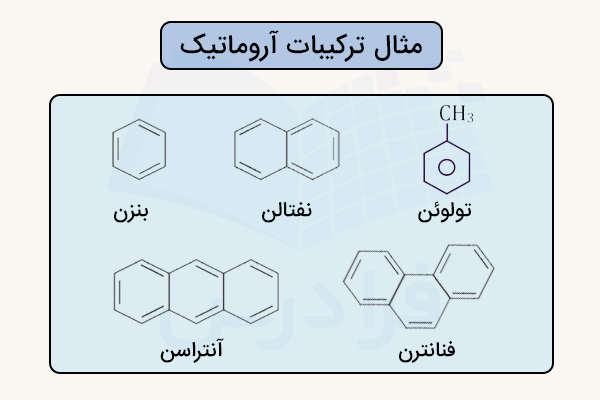
خواص ترکیبات آروماتیک
ترکیبات آروماتیک دارای نوع خاصی از پیوند هستند که بین پیوند یگانه و دوگانه قرار میگیرد. این ویژگی (ماهیت دوگانه جزئی) باعث پایداری بیشتر مولکول میشود. این ترکیبات نسبت به آلکنها واکنشپذیری کمتری دارند، زیرا پایداری بالایی دارند. به همین دلیل، به جای واکنشهای افزایشی، بیشتر در واکنشهای جانشینی شرکت میکنند، بدون اینکه ساختار حلقهای آنها تخریب شود.
از نظر تاریخی، بسیاری از این ترکیبات به دلیل بوی خاصشان نامگذاری شدهاند. برای مثال بنزن و نفتالین دارای بوی قابلتشخیص هستند، هرچند این ویژگی معیار علمی برای آروماتیسیته نیست. همچنین، ترکیبات آروماتیک به دلیل داشتن سیستمهای مزدوج پای، نور فرابنفش یا مرئی را جذب میکنند. این خاصیت در روشهای تجزیهای برای شناسایی و اندازهگیری این ترکیبات کاربرد دارد. پیشنهاد میکنیم برای شناخت بیشتر این نوع ترکیبات، فیلم آموزش آروماتیک چیست فرادرس که لینک آن در ادامه آورده شده است را مشاهده کنید.
واکنش ترکیبات آروماتیک
واکنشهای ترکیبات آروماتیک عمدتا از نوع جانشینی هستند، چون حلقه آروماتیک پایدار است و تمایلی به شکستن ساختار خود ندارد. در ادامه انواع این واکنشها را به صورت خلاصه نام میبریم.
- آروماتیزاسیون (Aromatization): تبدیل آلکانهای خطی به ترکیبات آروماتیک در دمای بالا و حضور کاتالیزور
- هالوژناسیون (Halogenation): جایگزینی یک هیدروژن حلقه با Cl یا Br با کمک کاتالیزور
- نیتراسیون (Nitration): جایگزینی هیدروژن با گروه با استفاده از اسید نیتریک و سولفوریک
- سولفوناسیون (Sulfonation): افزودن گروه به حلقه با اسید سولفوریک
- آلکیلاسیون فریدل-کرافتس (Friedel-Crafts Alkylation): افزودن گروه آلکیل به حلقه با و
- آسیلاسیون فریدل-کرافتس (Friedel-Crafts Acylation): افزودن گروه آسیل به حلقه با و
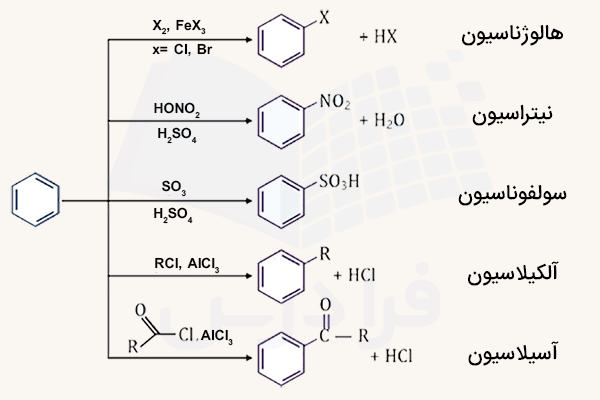
ترکیبات چندحلقهای آروماتیک
ترکیبات چند حلقهای آروماتیک (Poly Aromatic Hydrocarbons) ترکیباتی هستند که از به هم پیوستن چند حلقه آروماتیک تشکیل میشوند. در ادامه ساختار برخی از این ترکیبات را مشاهده میکنید.
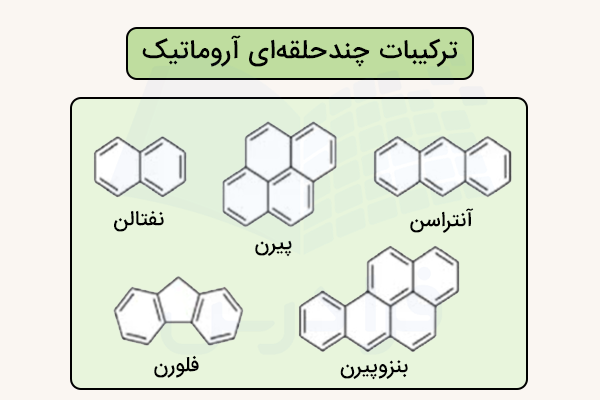
در این ترکیبات الکترونهای اوربیتالهای p روی چند حلقه پخش شده و پایداری بسیاری داشته باشند. این ترکیبات مانند نیمهرساناها عمل کرد و خواص اپتیکی و الکترونیکی ویژهای دارند. ترکیبات چند حلقهای آروماتیک در سلولهای خورشیدی یا دیودهای نوری نیز استفاده میشود. برخی از این ترکیبات مانند بنزوپیرنها، در اثر سوختن ناقص برخی از مواد مانند چوب، بنزین و نفت تولید شده و اثرات مخربی دارند.
این ترکیبات میتوانند سرطانزا باشند و بر روی DNA اثر بگذارند. ترکیبات چند حلقهای آروماتیک همچنین به سختی در طبیعت تجزیه میشوند به همین دلیل، از آلایندههای بسیار مهم آلی به شمار میآیند.
ترکیبات حلقوی غیر آروماتیک
هر ترکیب هیدروکربن حلقوی که قوانین آروماتیک بودن در آن صادق نباشد، یک ترکیب هیدروکربن حلقوی غیر آروماتیک است. ترکیبات غیرآروماتیک به مولکولهای آلی گفته میشود که خاصیت آروماتیسیته ندارند. آروماتیسیته ویژگی است که در مولکولهای حلقوی، مسطح و دارای سیستم الکترونی مزدوج دیده میشود و از قانون هوکل با فرمول تبعیت میکند. در مقابل، ترکیبات غیرآروماتیک فاقد یک یا چند مورد از این شرایط هستند و به همین دلیل، پایداری ویژه ترکیبات آروماتیک را ندارند.
این ترکیبات میتوانند به دو شکل باشند. یا زنجیر باز هستند مانند آلکانها، آلکنها و آلکینها، یا حلقوی هستند اما به دلیل نبود پیوستگی الکترونی یا غیرمسطح بودن، آروماتیک محسوب نمیشوند. این گروه از ترکیبات از نظر ساختاری بسیار متنوع هستند و در کاربردهای زیستی و صنعتی اهمیت زیادی دارند.
انواع ترکیبات شیمیایی حلقوی
در قسمتهای قبل آموختیم هیدروکربن حلقوی چیست. به طور کلی به مولکولی که یک یا چند حلقه داشته باشد، «ترکیب حلقوی» گفته میشود. اگر مولکولی دو یا چند حلقه داشته باشد، چه در یک سیستم حلقهای و چه در چند سیستم جداگانه، آن را «ترکیب چند حلقهای» مینامند. در مقابل، مولکولی که هیچ حلقهای نداشته باشد، «ترکیب غیرحلقهای» یا «زنجیر باز» نامیده میشود.
حلقه هم جنس یا هموسیکلیک به حلقهای گفته میشود که همه اتمهای آن از یک عنصر شیمیایی یکسان تشکیل شده باشند. در مقابل، حلقه ناهم جنس یا هتروسیکلیک حلقهای است که از اتمهای حداقل دو عنصر مختلف تشکیل شده باشد، یعنی حلقهای که همجنس نباشد. نوعی از حلقههای هم جنس، کربوسیکلیک است که در آن همه اتمها کربن هستند. از مهم ترین گروههای این نوع حلقه ها، حلقههای آلی حلقوی هستند و یکی از زیرگروههای مهم آنها سیکلوآلکانها هستند. در تصویر زیر برخی از ترکیبات هتروسیکل رسم شدهاند.
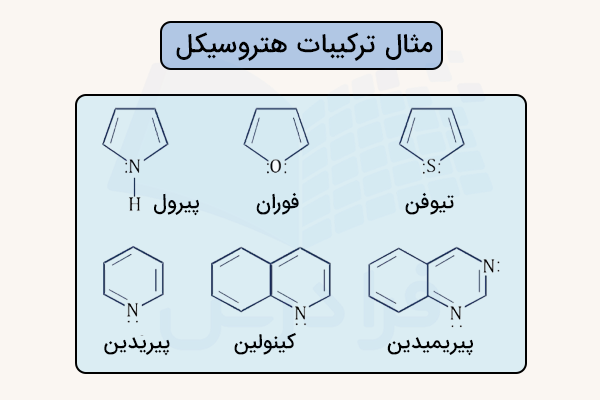
ترکیبات آلی حلقوی
سادهترین ترکیبات آلی حلقوی، سیکلوآلکانهای تکحلقهای هستند. این گروه شامل موادی مانند سیکلوپروپان، سیکلوبوتان، سیکلوپنتان، سیکلوهگزان، سیکلوهپتان و سیکلواوکتان و ترکیبات مشابه میشود. در کنار آنها، آلکانهای دوحلقهای نیز وجود دارند که از دو حلقه متصل به هم تشکیل شدهاند.
از مهمترین نمونههای آنها میتوان به دکالین، هوسان و نوربوران اشاره کرد. همچنین آلکانهای چندحلقهای ساختارهای پیچیدهتری دارند و نمونههایی مانند کوبان، بسکتان و تتراهدران را شامل میشوند. نوع دیگری از این ترکیبات، ترکیبات اسپیرو هستند. در این ساختارها، دو یا چند حلقه تنها از طریق یک اتم کربن مشترک به هم متصل میشوند، بنابراین حلقهها فقط یک نقطه اتصال دارند.
ترکیبات حلقوی غیرآلی
ترکیبات حلقهای فقط به ترکیبات آلی محدود نمیشوند و عناصر غیرآلی نیز میتوانند ساختارهای حلقهای تشکیل دهند. برای مثال، گوگرد میتواند ترکیب حلقهای «سیکلواکتاسولفور» (cyclooctasulfur) با فرمول را بسازد، یا ترکیباتی از نیتروژن، سیلیسیم، فسفر و بور نیز میتوانند حلقه تشکیل دهند، مانند «بورازین» (borazine) با فرمول که از نظر ساختار شبیه بنزن است.
در برخی موارد، اگر اتمهای کربن در ساختار بنزن با عناصر دیگر جایگزین شوند (مثل بور، سیلیسیم، ژرمانیم یا فسفر)، خاصیت آروماتیسیته همچنان حفظ میشود. به همین دلیل، ترکیبات حلقهای غیرآلی آروماتیک نیز وجود دارند و بهخوبی شناخته شدهاند.
تنش در هیدروکربن حلقوی چیست؟
هیدروکربنهای حلقوی به دلیل قرار گرفتن در ساختار حلقه و تغییرات زاویه پیوندی آنها همواره دارای مقداری تنش هستند. این تنش میتواند بر مقدار پایداری این ترکیبات اثر بگذارد. برای مثال، ترکیبات حلقوی سه کربنی به دلیل کوچک بودن زاویه پیوندی تنش زیادی داشته و نسبت به ترکیبات حلقوی ۶ کربنی کمتر پایدارند.
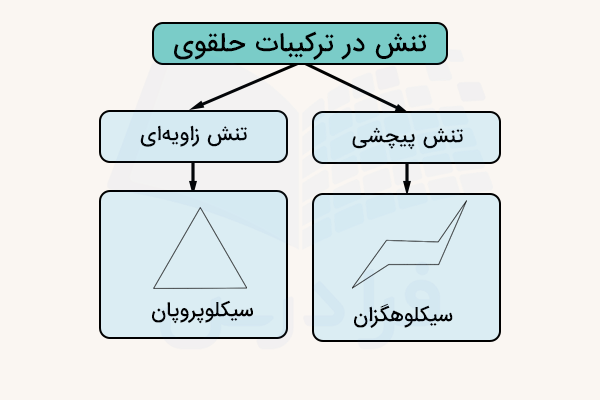
تنش در ترکیبات حلقوی میتواند از دو نوع تنش زاویهای یا تابشی (پیچشی) باشد. در ادامه این موارد را توضیح میدهیم.
تنش زاویه ای
تنش زاویهای در ترکیباتی که حلقههای بسیار بزرگ (بیش از ۷ یا ۸ اتم) یا بسیار کوچک (کمتر از ۵ اتم) دارند، وجود دارد. در این ترکیبات این تنش باعث ناپایداری ترکیب حلقوی میشود. برای مثال در ترکیب سیکلوپروپان که یک نوع آلکان حلقوی است، زاویه پیوندی ۶۰ درجه است در حالی که زاویه پیوندی ایدهآل برای این ترکیب با توجه به جایگاه اتمها و الکترونها، ۱۰۴ درجه است.
تنش تابشی یا پیچشی
تنش تابشی یا پیچشی در ترکیبات حلقوی که در آنها پیوندها یا اتمها در محورهای مختصات روی هم قرار میگیرند وجود دارد. این پدیده باعث ایجاد دافعه بین الکترونها و ناپایداری ترکیب میشود.
برای مثال در ترکیب سیکلوهگزان به دلیل وجود ۲ اتم هیدروژن بر هر اتم کربن، تنش پیچشی به وجود میآید. به همین دلیل ، ساختار سیکلوهگزان از فرم صفحهای خارج شده و فرم صندلی به خود میگیرد تا مقدار تنش آن کاهش یافته و پایدار شود. این فرم در تصویر زیر مشخص شده است.
محاسبه تنش هیدروکربن حلقوی
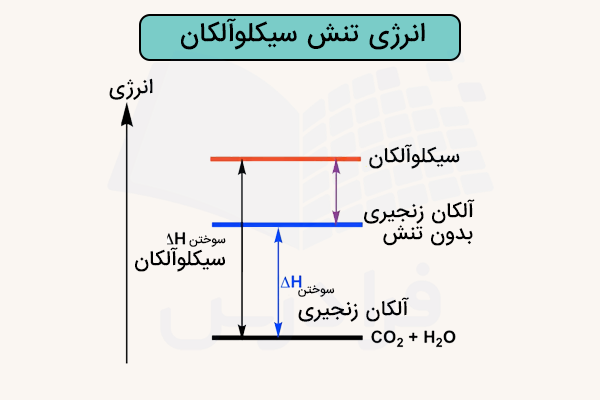
در قسمت قبل آموختیم تنش در هیدروکربن حلقوی چیست. هیدروکربنهای حلقوی مانند سایر هیدروکربنها میسوزند و گرما و حرارت قابل توجی آزاد میکنند. هیدروکربنهای حلقوی در صورت سوختن، باز شده و تنش آنها از بین میرود. در نتیجه باز شدن حلقه و از بین رفتن تنش، انرژی مقدار تنش به شکل انرژی گرمایی آزاد میشود.
بنابراین با اندازهگیری میزان آنتالپی سوختن این هیدروکربنها ومقایسه آن با آنتالپی سوختن هیدروکربنهای راست زنجیر مشابه آنها (با همان تعداد اتم کربن)، میتوان مقدار انرژی تنش را محاسبه کرد. هرچه میزان انرژی تنش بیشتر باشد، میزان تنش در آن ترکیب بیشتر بوده است. این اختلاف انرژی سوختن در تصویر زیر برای ترکیبات سیکلوآلکان مشخص شده است.
کرنش ترکیبات هیدروکربن حلقوی چیست؟
در شیمی آلی، «کرنش حلقهای» (ring strain) نوعی ناپایداری است که وقتی زاویههای پیوند در یک مولکول (به دلیل قرار گرفتن در ساختار حلقهای) از مقدار طبیعی خود منحرف شوند، ایجاد میشود. این پدیده بیشتر در حلقههای کوچک مانند سیکلوپروپان و سیکلوبوتان دیده میشود، زیرا زاویههای داخلی آنها از مقدار ایدهآل حدود ۱۰۹ درجه کوچکتر است. به همین دلیل، این ترکیبات انرژی بیشتری (مثلا گرمای سوختن بالاتر) دارند.
کرنش حلقهای از چند عامل به وجود میآید:
- کرنش زاویهای (انحراف از زاویه ایدهآل)
- کرنش پیچشی یا پیتزر (همپوشانی پیوندها)
- کرنش ترانسآنولار (برهمکنش اتمهای روبهرو در حلقه)
انرژی کرنش حلقهای در واقع ناشی از انرژی لازم برای تغییر طول و زاویه پیوندها جهت تشکیل حلقه است.
تفاوت تنش و کرنش هیدروکربن حلقوی چیست؟
در شیمی آلی، کرنش به تغییر واقعی در ساختار هندسی یک مولکول گفته میشود. این تغییر زمانی رخ میدهد که به دلیل قرار گرفتن اتمها در یک حلقه، زاویهها یا آرایش فضایی پیوندها از حالت ایدهآل خود (مثلا حدود ۱۰۹ درجه) برای کربن منحرف شوند. به عنوان مثال در سیکلوپروپان، زاویههای پیوندی به حدود ۶۰ درجه میرسند که نشاندهنده مقدار زیادی کرنش زاویهای در ساختار است. بنابراین کرنش در واقع توصیفکننده میزان تغییر شکل هندسی مولکول است.
در مقابل، تنش به اثر انرژی این تغییر شکل اشاره دارد. یعنی وقتی کرنش در ساختار ایجاد میشود، مولکول ناپایدارتر شده و انرژی آن افزایش پیدا میکند. این افزایش انرژی همان تنش است که باعث میشود مولکول تمایل بیشتری به واکنشپذیری داشته باشد. به طور خلاصه، کرنش خود تغییر هندسی است، در حالی که تنش نتیجه انرژی و ناپایداری ناشی از آن تغییر شکل محسوب میشود.
استریوشیمی هیدروکربن حلقوی
تشکیل حلقه در مولکولها میتواند باعث قفل شدن موقعیت برخی اتمها و گروههای عاملی شود و در نتیجه پدیدههایی مانند استریوشیمی و کایرالیته به وجود آید. این موضوع در ترکیبات حلقهای اهمیت بیشتری دارد، زیرا برخی ایزومرهای فضایی (مثل ایزومرهای پیکربندی) مخصوص همین ساختارها هستند.
همچنین، حلقهها میتوانند شکلهای فضایی مختلفی داشته باشند که به آن ایزومری کنفورماسیونی گفته میشود. برای مثال، سیکلوهگزان بین دو شکل اصلی صندلی و قایقی در حال تعادل است. حالت صندلی پایدارتر است، زیرا در آن تنش زاویهای، پیچشی و فضایی کمتر است.
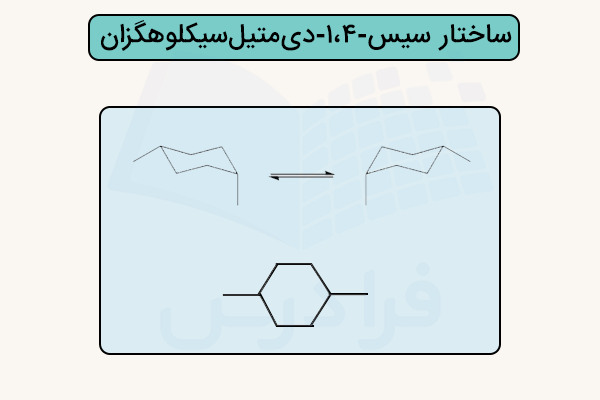
در سیکلوهگزانهای جانشیندار، نوع و موقعیت جانشینها تعیین میکند کدام کنفورماسیون غالب باشد. گروههای حجیم معمولا ترجیح میدهند در موقعیت استوایی قرار بگیرند تا از تنش فضایی دور باشند. برای مثال، در سیس-۱،۴-دیمتیلسیکلوهگزان (cis-1,4-dimethylcyclohexane)، دافعه بین دو گروه متیل باعث میشود فرم صندلی پایدارتر از فرم قایقی باشد.
نمایش هیدرو کربنهای حلقوی
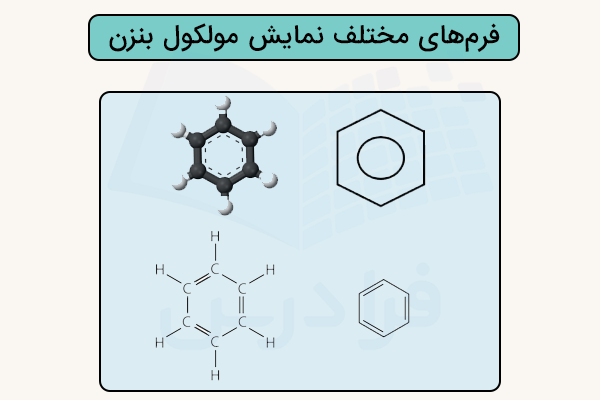
فرمولهای ساختاری هیدروکربنهای حلقهای را میتوان به چند روش نمایش داد. در یک روش، تمام اتمها و پیوندها بهصورت کامل نشان داده میشوند. در روش سادهتر، نماد اتمها حذف میشود و فقط شکل هندسی نمایش داده میشود، مثلا یک مثلث که رأسهای آن نشاندهنده اتمهای کربن هستند.
در تصویر زیر شکل ساختار بنزن به روشهای مختلف نمایش داده شده است. در ترکیبات آروماتیک، اغلب برای سادهسازی ساختار و نمایش رزونانس، دارهای به جای پیوندهای دوگانه درون حلقه رسم میشود. در تصویر زیر مشخص شده است فرمهای مختلف نمایش هیدروکربن حلقوی بنزن چیست.
یادگیری شیمی آلی با فرادرس
برای درک بهتر این مفهوم که هیدروکربن حلقوی چیست، ابتدا باید با مفاهیمی چون ایزومر فضایی، رزونانس، گروه عاملی، شیمی فضایی، فعالیت نوری، واکنشهای حذفی، واکنشهای جانشینی هسته دوست و ... آشنا شویم. پیشنهاد میکنیم برای یادگیری بهتر این مفاهیم، به مجموعه فیلم آموزش شیمی فرادرس از دروس دانشگاهی تا کاربردی مراجعه کنید که با زبانی ساده ولی کاربردی به توضیح این مفاهیم میپردازد.
همچنین، با مراجعه به فیلمهای آموزش فرادرس که در ادامه آورده شده است میتوانید به آموزشهای بیشتری درباره هیدروکربن حلقوی دسترسی داشته باشید.
- فیلم آموزش شیمی آلی ۲ مرور و حل مساله
- فیلم آموزش شیمی تجزیه ۲ مرور و حل مساله
- فیلم آموزش کاربرد طیف سنجی در شیمی آلی و مرور و حل تست کنکور ارشد
واکنش ترکیبات هیدروکربن حلقوی
برای تشکیل و تغییر ساختار حلقهها در شیمی آلی، واکنشهای سنتزی متنوعی وجود دارد که به سه دسته کلی تقسیم میشوند. این واکنشها تشکیل حلقه، باز شدن حلقه و تغییر اندازه حلقه هستند. در قسمت بعد میآموزیم واکنشهای ترکیبات هیدروکربن حلقوی چیست.
واکنش باز شدن حلقه در هیدروکربن حلقوی
یکی از مهمترین واکنشهایی که در ترکیبات حلقوی صورت میگیرد، واکنش باز شدن حلقه (Ring Opening) است. این واکنش به خصوص در ترکیبات حلقوی کوچک مانند سیکلوپروپان اهمیت ویژهای دارند.
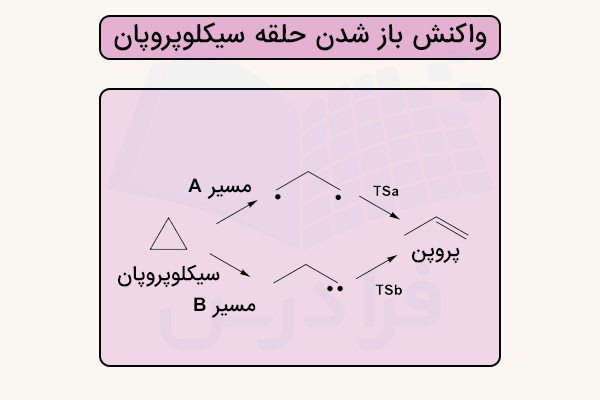
این ترکیبات در حضور اسید یا کاتالیزور فلزی، یکی از پیوندهای آنها شکسته و حلقه آنها باز میشود. الکترونهای حاصل از باز شدن حلقه میتواند پیوند دوگانه تشکیل داده یا به مواد دیگر متصل شود. در نتیجه مولکول از ساختار حلقوی خارج شده، تنش آن کم شده و ساختار پایدارتری میگیرد.
واکنشهای تشکیل حلقه در هیدروکربن حلقوی
در این واکنشها، یک مولکول خطی یا زنجیری به گونهای تغییر میکند که دو انتهای آن به هم متصل شده و یک حلقه تشکیل میشود. این فرایند یکی از مهمترین روشها برای ساخت ترکیبات حلقهای است و معمولا با کنترل شرایط، اندازه حلقه و آرایش فضایی آن نیز قابل تنظیم است.
این واکنشها معمولا یکی از موارد زیر هستند.
- تراکم آسیلوئین: در این واکنش، دو گروه کربونیل (معمولا استرها) در حضور فلز سدیم به هم متصل میشوند و یک حلقه به همراه یک گروه هیدروکسیکتون (آسیلوئین) تشکیل میدهند.
- دایکمن: تراکم درونمولکولی دیاسترها در حضور باز که منجر به تشکیل حلقههای پنج یا شش عضوی و تولید بتا-کتواستر میشود.
- دیلز - آلدر: واکنش همزمان دیان و آلکن که یک حلقه ششعضوی با کنترل استریوشیمی بالا ایجاد میکند.
- متاتز حلقهزا: اتصال دو انتهای آلکن در حضور کاتالیزور فلزی و تشکیل حلقه که واکنشی با بازده بالا و قابلیت کنترل اندازه حلقه است.
- سیکلیزاسیون رادیکالی: ایجاد رادیکال درون مولکول که به بخش دیگر حمله کرده و حلقههای پیچیده و چندمرحلهای را تشکیل میدهد.
واکنشهای تغییر اندازه حلقه
در این واکنشها، اندازه حلقه بدون از بین رفتن کامل ساختار اصلی تغییر میکند. این تغییر میتواند به دلیل ورود یک اتم جدید (انبساط) یا حذف یک بخش از حلقه (انقباض) یا بازآرایی درون مولکولی رخ دهد و برای تنظیم پایداری یا ساختار نهایی بسیار مهم است.
- انبساط حلقه: افزایش اندازه حلقه از طریق وارد شدن یک اتم یا گروه (مثل در واکنش بایر–ویلیگر که اکسیژن وارد حلقه میشود و کتون به استر تبدیل میشود.)
- انقباض حلقه: کاهش اندازه حلقه از طریق حذف یک اتم یا بازآرایی ساختاری که معمولا در شرایط خاص یا با واسطههای ناپایدار انجام میشود.
- بازآراییهای حلقه: تغییر چیدمان اتمها درون حلقه بدون شکستن کامل آن که میتواند باعث تغییر شکل یا اندازه نسبی حلقه شود.
جمعبندی
در این مطلب از مجله فرادرس آموختیم مفهوم هیدروکربن حلقوی چیست. ترکیبات هیدروکربن حلقوی ترکیباتی هستند که از کربن و هیدروژن تشکیل شده و ساختاری حلقوی دارند. این ترکیبات میتوانند تک حلقهای یا چند حلقهای باشند و همچنین میتوانند پیوندهای یگانه، دوگانه یا سهگانه داشته باشند.
به دلیل تشکیل حلقه در این ترکیبات، تنش و کرنش حلقه باعث ناپایداری آنها شده و در بین این ترکیبات، هیدروکربنهای آروماتیک که ساختاری مسطح دارند، پایدارتر هستند. ترکیبات حلقوی در واکنشهای مختلفی مانند واکنش باز شدن حلقه، حلقهزایی و واکنش دیلز - آلدر شرکت میکنند.












